Here is another study that announces exceptional results "A daily fiber supplement improved brain function in people over 60 in just 12 weeks!"
The scientists are raving in the press kit: "We are excited to see these changes in just 12 weeks. This holds huge promise for enhancing brain health and memory in our aging population." says first author Dr. Mary Ni Lochlainn from the Department of Twin Research.
Yet other studies have previously shown limited evidence that probiotics may improve cognition in older people with pre-existing cognitive impairment but no clear evidence of the benefit on physical function, frailty, mood, length of hospitalization, and mortality.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7515554/
 Improving cognition using a simple probiotic would be an extraordinary result due to its simplicity of implementation.
Improving cognition using a simple probiotic would be an extraordinary result due to its simplicity of implementation.
In this study, as in almost all studies, we do not know what led the scientists to test the effect of a molecule. Here the authors wanted to boost the muscle mass of elderly twins (over 60 years old).
Both twins consumed a protein (BCAA) supplement powder, and in one twin from each pair, this was combined with a prebiotic supplement 7.5 g of prebiotic (Darmocare Pre®, Bonsuvan), which consists of inulin (3.375 mg) and fructo-oligosaccharides (FOS) (3,488 mg) and in the other twin from each pair, it was combined with a placebo (maltodextrin). As the products were sent by postal service, it is not known to what extent the treatment was correctly administered. Similarly, it was the patients measured by themselves their performance on the tests. The gender of the patients was not collected but it is assumed as they were elderly patients, that the cohort is majority female.
Stool samples were collected by the participants themselves using the sample collection kits provided. Twins were asked to collect a “pea-sized” stool sample into a DNA/RNA Shield Faecal Collection Tube (Zymo Research), and these were posted to the laboratory.
There is a strong recruitment bias (as usual): Participants were eligible for inclusion if they were aged 60 years or older and had previously reported low dietary protein intake (<1 g/kg body weight/day).
However, when we look at the results, it seems they are very different from what is advertised (as usual).
The results are generally the same in the two groups, with even an improvement in the chair rise test, contrary to what is announced. This improvement is even greater in the placebo group! Could this be attributed to the administration of maltodextrin in the placebo group?
Reviews have concluded that digestion-resistant maltodextrin is classified as a type 5 resistant starch (RS5), a prebiotic dietary fiber having properties that may improve the management of diabetes and other disorders of metabolic syndrome. The action of maltodextrin could be quite similar to that of the BCAAs used in the treatment group.
For the CANTAB test, there is improvement in both groups, but the improvement is greater in the treatment group. However, a standard deviation of 0.83 indicates that the results were indeed highly variable from one patient to the next, highlighting the heterogeneity of responses within the study population.
Furthermore, at the start of the study, the treatment group did not seem to be already impacted by cognitive problems while this was already the case for the placebo group, which raises questions about the objectivity of the random distribution between the two groups.
For the latency test (response speed) both groups progressed, but the treatment group progressed more.
For the Spatial working memory test, it is the placebo group that progresses the most!
For the PAL test: first attempt memory score, it is the treatment group which progresses the most (but as for the previous test both groups progress)
For the Pattern recognition memory test, both groups progressed, but the treatment group progressed more.
For the Spatial span (forward span length) test, the treatment group progressed, but the placebo group regressed.
In conclusion, the study announces exceptional results, but the results are minimal, and above all, they may be because the investigators supplemented a group of patients who had been selected as being undernourished with protein. Both groups received compounds that are sugars in the broad sense.


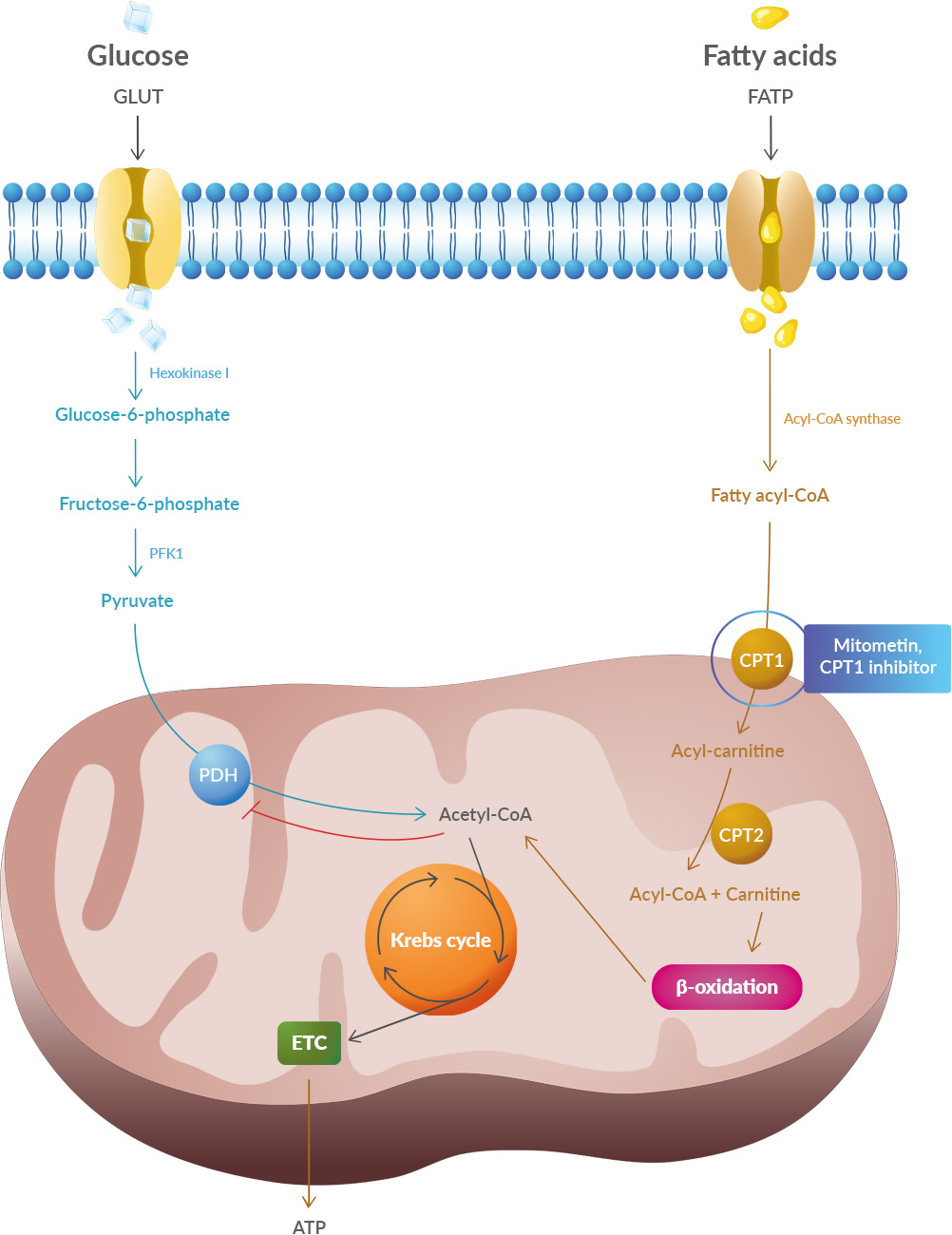 Studies have shown that oxidative stress and endoplasmic reticulum stress are correlated and can lead to protein misfolding (Abramov et al., 2020). Accumulation of misfolded proteins causes cellular damage and mitochondrial dysfunction and is associated with a range of neurodegenerative diseases, including ALS (misfolded SOD1, TDP-43, C9orf72) (McAlary et al., 2020), Parkinson's disease (misfolded α-synuclein) and Alzheimer disease (misfolded Aβ and Tau) (Abramov et al., 2020).
Studies have shown that oxidative stress and endoplasmic reticulum stress are correlated and can lead to protein misfolding (Abramov et al., 2020). Accumulation of misfolded proteins causes cellular damage and mitochondrial dysfunction and is associated with a range of neurodegenerative diseases, including ALS (misfolded SOD1, TDP-43, C9orf72) (McAlary et al., 2020), Parkinson's disease (misfolded α-synuclein) and Alzheimer disease (misfolded Aβ and Tau) (Abramov et al., 2020).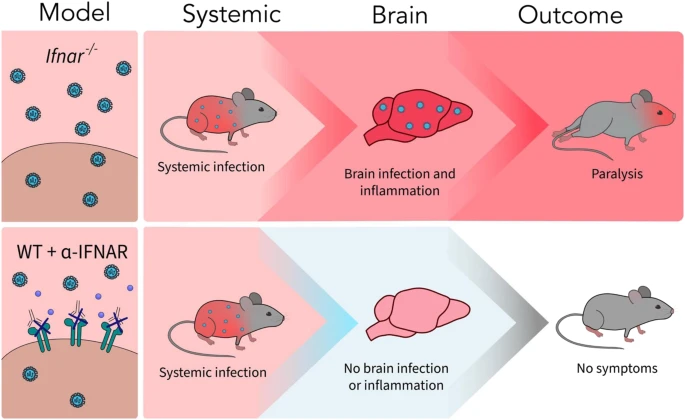 A new article aims to show that in the case of Zika viruses,
A new article aims to show that in the case of Zika viruses, 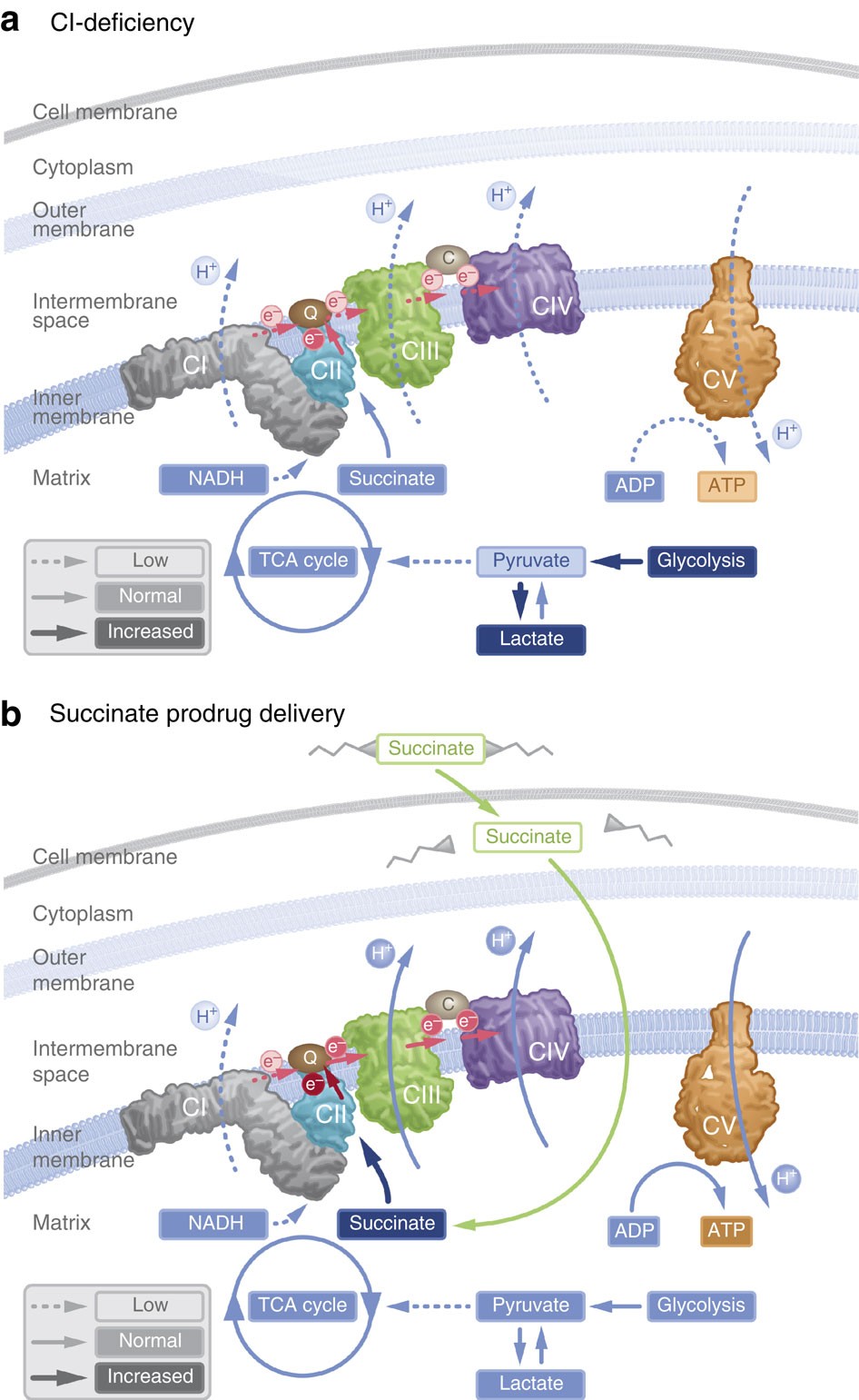 In particular, supplementation with dimethyl succinate, a substrate bypassing the inhibited step in the TCA cycle, suggests a potential therapeutic strategy to mitigate mitochondrial dysfunction in Alzheimer's disease. Dimethyl succinate (DMS), a membrane-permeant form of succinate, could serve as a pro-drug to provide substrate to the next enzymatic step in the TCA cycle, succinate dehydrogenase (SDH).
In particular, supplementation with dimethyl succinate, a substrate bypassing the inhibited step in the TCA cycle, suggests a potential therapeutic strategy to mitigate mitochondrial dysfunction in Alzheimer's disease. Dimethyl succinate (DMS), a membrane-permeant form of succinate, could serve as a pro-drug to provide substrate to the next enzymatic step in the TCA cycle, succinate dehydrogenase (SDH). The authors believe that an impaired blood-brain barrier allows immune cells from the body to pass through, which leads to the activation of microglia in the central nervous system. Scientists point out that immune processes intensively consume energy, therefore glucose, and therefore insulin resistance slows down immune processes.
The authors believe that an impaired blood-brain barrier allows immune cells from the body to pass through, which leads to the activation of microglia in the central nervous system. Scientists point out that immune processes intensively consume energy, therefore glucose, and therefore insulin resistance slows down immune processes. .
(source:
.
(source:  Nos précédentes publications sur ce site, avertissaient déjà que cette révision aurait pour conséquence principale que les essais cliniques de médicaments seraient majoritairement approuvés, alors que la totalité des essais cliniques (324 de phase III) sur la maladie d’Alzheimer (y compris les médicaments récemment autorisés) se sont soldés par des échecs, et parfois par des effets secondaires dramatiques (ARIA).
Nos précédentes publications sur ce site, avertissaient déjà que cette révision aurait pour conséquence principale que les essais cliniques de médicaments seraient majoritairement approuvés, alors que la totalité des essais cliniques (324 de phase III) sur la maladie d’Alzheimer (y compris les médicaments récemment autorisés) se sont soldés par des échecs, et parfois par des effets secondaires dramatiques (ARIA).