Le vieillissement est un processus complexe qui affecte tous les humains, et qui s'accompagne d'une susceptibilité accrue à une gamme large de maladies, notamment neurodégénératives.
Aussi dans le cadre de ces maladies neurodégénératives, plutôt que de viser une cible thérapeuthique moléculaire comme TDP-43 pour la SLA ou alpha-synucléine pour la maladie de Parkinson, pourquoi ne peut vouloir rajeunir les cellules et les tissus qu'elles composent?
De nombreuses études indiquent que le processus de vieillissement n'est peut-être pas aussi inévitable qu'on le pensait auparavant.
Parmi les interventions connues qui aboutissent à un vieillisssement ralenti, on trouve la parabiose. Il en effet été démontré que le sang de sujets jeunes a des propriétés rajeunissantes. La parabiose est une technique dans laquelle les systèmes circulatoires deux organismes, l'un jeune et l'autre âgé sont connectés.
Une autre technique élimine des cellules sénescentes, retarde l'apparition de pathologies liées à l'âge et peut prolonger la durée de vie. Par conséquent, les médicaments appelés sénolytiques qui induisent sélectivement l'apoptose dans les cellules sénescentes font l'objet de recherche intenses dans le domaine du vieillissement moléculaire. Bien sûr il est hors de question d'appliquer cette technique à des cellules qui se renouvellent lentement (comme les muscles) voire pas du tout comme les neurones moteurs ce qui serait catastrophique pour des malades de la SLA.
La manipulation de l'apport alimentaire est également l'une des interventions de vieillissement les plus étudiées. Divers régimes (par exemple restriction calorique, jeûne intermittent, régime cétogène) manipulent les voies de détection des nutriments, en particulier celles impliquant mTOR et l'insuline/facteur de croissance analogue à l'insuline (IGF), pour prolonger la durée de vie et réduire les facteurs de risque métaboliques. Divers médicaments, tels que la rapamycine, semblent imiter les effets de la restriction calorique et induisent l'autophagie. Là encore il semble impossible d'appliquer de telles techniques à des maladies dont on sait qu'elles sont caractérisées pour des anomalies métaboliques graves.
Un apport récent aux stratégies anti-âge en cours de développement, vient des approches de reprogrammation cellulaire. Contrairement à des affirmations dogmatiques faites au cours du siècle précédent, que les phénotypes cellulaires des cellules matures, ne sont pas irréversibles, elles peuvent êtres manipulées vient des interventions chimiques. C'est ce qu'on appelle la reprogrammation cellulaire.
Les cellules souches embryonnaires sont les cellules centrales du développement, puisqu'elles vont générer progressivement toutes les autres cellules de l'organisme, grâce à des étapes de différenciation et de prolifération finement orchestrées pour créer, finalement, un individu pluricellulaire viable. Cependant chez l'adulte des cellules souches sont toujours actives et permettent la création continue de muqueuses, de peau, de sang. En général la création de cellules matures passe par différentes étapes. Par exemple au cours du processus de maturation des globules rouges, un hémocytoblaste, une cellule souche hématopoïétique multipotente, génère des progéniteurs myéloïdes commun ou cellule souche multipotente, puis une cellule souche unipotente, puis un basophile, aussi communément appelé érythroblaste, puis un réticulocyte (un globule rouge immature) qui va quitter la moëlle osseuse pour intégrer la circulation sanguine.
Cependant, la reprogrammation cellulaire transforme une cellule en un état pluripotent, où elle a le potentiel de générer n'importe quel type de cellule somatique. Ce procédé n'est pas approprié pour une thérapie anti-âge in vivo car il nécessite non seulement la perte de l'identité cellulaire originelle, ce qui reviendrait à tuer l'hôte biologique par arrêt des différents organes. De plus, l'induction de la pluripotence ou l'injection directe de cellules pluripotentes in vivo conduisent invariablement au cancer chez la souris. Pour qu'une intervention basée sur la reprogrammation cellulaire soit considérée comme rajeunissante (transformation d'une vieille cellule en une cellule plus jeune), l'identité des cellules somatiques doit être impérativement conservée.
Cellules souches pluripotentes induites:
Les travaux révolutionnaires de Takahashi et Yamanaka en 2006 ont montré que la surexpression de quatre facteurs de transcription (Oct3/4, Sox2, Klf4 et c-Myc, désormais appelés « facteurs Yamanaka » ou facteurs « OSKM ») réorganise le paysage épigénétique et convertit les cellules somatiques en un état pluripotent. Depuis la création de cellules souches pluripotentes induites (iPSC) in vitro, il est devenu clair que l'identité cellulaire est dictée par des changements épigénétiques, plutôt que par la perte ou les altérations de l'ADN génomique. Les conséquences de cette découverte n'ont probablement pas encore été complètement assimilées tant est encore forte l'idée que le génome contient toutes les informations qui définissent la cellule.
Les iPSC offrent la promesse d'une thérapie régénérative dirigée et personnalisée (c'est-à-dire les iPSC cultivés à partir de cellules de patients, minimisant l'incompatibilité) pour des maladies actuellement incurables, telles que les maladies neurodégénératives du système nerveux central, l'infarctus du cœur, le diabète sucré, ainsi que le foie, les poumons, et variétés de maladies rénales. Il s'agit là véritablement de la nouvelle frontière en matière de médecine, car ces maladies sont pour l'instant réfractaires à tout traitement qui ne serait pas seulement symptomatique.
Rajeunissement épigénétique induit par la reprogrammation
La reprogrammation des cellules vers la pluripotence a montré qu'en principe, les phénotypes cellulaires liés à l'âge peuvent être inversés, y compris dans les cellules différenciées en phase terminale qui ne se divisent pas. Cependant, cela est basé sur la dédifférenciation, transformant les cellules en un état semblable à celui des cellules souches, en tant que processus sous-jacent. La dédifférenciation est également un processus observé dans l'oncogenèse (le début du processus de cancérisation). Pour éviter le risque d'induction de cancer, une autre stratégie a été proposée : le rajeunissement épigénétique - où une vieille cellule est rajeunie sans changement d'identité cellulaire.
Si, par exemple, l'inversion de l'âge lors de la reprogrammation cellulaire pouvait être découplée de la dédifférenciation, une stratégie de rajeunissement viable à l'abri du risque de cancer pourrait exister. Pour obtenir un rajeunissement épigénétique via des facteurs de reprogrammation, il est nécessaire d'interompre le processus à un stade intermédiaire, où les cellules ont commencé à changer épigénétiquement, mais ne se sont pas encore complètement dédifférenciées.
Les cellules sont ainsi isolées entre les jours 3 et 15 au cours de la dédifférenciation induite par l'OSKM humain classique alors qu'elles n'ont pas encore perdu leur identité somatique. Une tentative pilote de test conceptuel du rajeunissement épigénétique a été faite par Manukyan et al. où OSKM + LIN28 a été exprimé dans des fibroblastes sénescents humains et la mobilité de la protéine d'hétérochromatine 1β (HP1β) a été restaurée à des niveaux non sénescents, mais pas aux niveaux de cellules souches embryonnaires humaines (CSEh).
De plus, Ocampo et al. ont démontré qu'une reprogrammation partielle, obtenue par induction transitoire et périodique d'OSKM (2 jours de traitement, puis 5 jours de repos, répétée plusieurs fois), améliore les signes du vieillissement sans perte d'identité cellulaire. Ils ont d'abord effectué une reprogrammation partielle sur des fibroblastes de souris progéroïdes (a viellissement accéléré) et atténué les caractéristiques associées à l'âge, telles que les dommages à l'ADN, les dommages à l'enveloppe nucléaire, la dérégulation des modifications des histones, les facteurs associés au stress et à la sénescence et les espèces réactives de l'oxygène (ROS ).
Un rajeunissement similaire des modifications d'histones dérégulées a également été observé lorsqu'une reprogrammation transitoire a été effectuée sur des fibroblastes humains à passage élevé (dérivés d'iPSC). Une reprogrammation partielle a également été appliquée in vivo à des souris progéroïdes, ce qui a prolongé leur durée de vie en l'absence de formation de tératome. Lorsqu'il est répété chez des souris d'âge mûr naturellement âgées, la capacité de régénération des muscles et du pancréas après une blessure a été améliorée, ainsi que la tolérance au glucose.
Depuis l'OSKM exprimé de manière transitoire chez la souris par Ocampo et al., la reprogrammation partielle est devenue une avenue passionnante pour la recherche sur le rajeunissement. Ce qui restait également peu clair était la nature du rajeunissement qui se produisait.
Pour tester ces scénarios, deux biomarqueurs sont nécessaires pour suivre:
(i) le vieillissement biologique
(ii) l'état de dédifférenciation.
 Les chercheurs ont appliqué divers prédicteurs d'âge à une reprogrammation bien étudiée de 49 jours sur des fibroblastes dermiques humains (HDF) qui contenaient à la fois des données de méthylation (pour suivre l'âge comme indicateur de l'âge biologique) et des données d'expression génique (pour suivre les marqueurs cellulaires comme un proxy pour l'identité somatique).
Les chercheurs ont appliqué divers prédicteurs d'âge à une reprogrammation bien étudiée de 49 jours sur des fibroblastes dermiques humains (HDF) qui contenaient à la fois des données de méthylation (pour suivre l'âge comme indicateur de l'âge biologique) et des données d'expression génique (pour suivre les marqueurs cellulaires comme un proxy pour l'identité somatique).
Le rajeunissement de l'âge commence après le jour 3 et diminué régulièrement jusqu'à atteindre l'age zéro au jour 20, bien avant la fin de la chronologie de reprogrammation. Pendant ce temps, l'expression du gène marqueur des fibroblastes diminuée et reste à des niveaux relativement stables jusqu'au jour 15, après quoi elle a chuté de façon spectaculaire.
Ainsi, la majorité des cellules du jour 15 sont au-delà du "point de non-retour" et dans la phase de maturation de la reprogrammation, où la mémoire de leur identité cellulaire d'origine est perdue. Il y a une fenêtre où la réjuvénation semble possible et sans danger entre les jours 3 et 13. Cette technique est-elle réellement applicable à des sujets agées, la réjuvénaton éventuelle est-elle permanente, quel est le risque de cancer?
Une prépublication récente de Gill et al. ont abordé ces questions en utilisant un système de reprogrammation in vitro similaire avec des fibroblastes de donneurs d'âge moyen et en arrêtant l'expression d'OSKM après les jours 10, 13, 15 ou 17. L'étude a confirmé un phénotype rajeuni des cellules reprogrammées de manière transitoire, qui est maintenu lors du retour à l'état somatique au moins quatre semaines après le retrait de l'OSKM. Ces cellules ont conservé leur phénotype plus juvénile et ont montré un âge transcriptionnel moins dégradé que celui de leur âge biologique, une expression génique associée à l'âge régulée à la baisse et une expression régulée à la hausse des gènes caractéristiques des cellules plus jeunes telles que les collagènes.
Les auteurs ont défini le jour 13 comme un "sweet spot" pour le rajeunissement, où l'âge a été réduit d'environ 30 ans après le retrait de l'OSKM. Cette observation est cohérente avec les données d'Ohnuki et al pour le jour 13 avant le retrait de l'OSKM, qui coïncide également avec la limite de « fenêtre de sécurité » partiellement reprogrammée définie dans Olova et al. De plus, Gill et al. montrent que les activateurs spécifiques aux fibroblastes sont restés déméthylés pendant l'exposition transitoire à l'OSKM, agissant ainsi comme un support de mémoire épigénétique pour l'identité des fibroblastes et facilitant le retour à l'état somatique.
Pendant la fenêtre de reprogrammation partielle, les gènes somatiques maintiendraient une expression plus faible mais stable, pointant vers un programme de transcription qui est "en attente" et pas encore perdu.
D'autres études ont confirmé et étendu les observations précédentes. Sarkar et al. ont exprimés par thérapie mARN, OSKM + LIN28 + NANOG (OSKMLN) de manière transitoire dans des fibroblastes dermiques humains adultes et des cellules endothéliales pendant quatre jours et ont analysé l'expression et la méthylation des gènes deux jours après l'interruption (Ocampo et al., en comparaison, ont utilisé un système inductible par la doxycycline et une expression forcée 2–4 jours dans des cultures cellulaires). Une caractéristique importante de ce système est que l'OSKMLN est introduit de manière non intégrative sous la forme d'un cocktail de molécules d'ARNm, ce qui signifie qu'il n'y a pas d'intégration aléatoire d'OSMKLN dans le génome, ce qui minimise le risque oncogénique.
Ils ont comparé l'âge et l'expression de l'ARN d'échantillons âgés (60 à 90 ans) avant et après traitement, avec des échantillons jeunes (15 à 35 ans). Selon l'horloge de Horvath, le traitement OSKMNL a significativement réduit l'âge des fibroblastes et des cellules endothéliales, bien que l'effet ait été plus prononcé dans ces dernières.
Sarkar et al. ont ensuite testé l'effet de la reprogrammation partielle sur les cellules souches en transplantant des cellules souches musculaires squelettiques (MuSC) âgées, jeunes, âgées et transitoires, traitées à l'OSKMNL, dans les muscles blessés de souris immunodéprimées. Ils ont observé une capacité de régénération améliorée dans les anciens MuSC traités à l'OSKMNL, comparable à celle des jeunes MuSC, et aucun tératome ou lésion néoplasique ne s'est développé. Une amélioration de la fonction musculaire a également été observée dans les muscles greffés avec les anciens MuSC traités à l'OSKMNL par rapport aux anciens MuSC non traités. Sarkar et al. ont répété l'expérience avec des MuSC humains âgés (60 à 80 ans) et ont constaté qu'ils avaient également une capacité de prolifération supérieure à celle des cellules non traitées, comparable aux jeunes MuSC humains. Cela semble de bonne augure pour les malade de la SLA.
Une autre approche de reprogrammation cellulaire a récemment été testée dans les troubles de la vision liés à l'âge et aux blessures chez la souris. Lu et al. ont montré que l'expression ectopique d' Oct4, Sox2 et Klf4 (OSK) stimulait la régénération des axones dans un modèle murin de lésion par écrasement du nerf optique. La même stratégie a conduit à une vision améliorée dans un modèle murin de glaucome. Le traitement OSK chez des souris saines âgées de 12 mois a amélioré l'acuité visuelle et l'expression des gènes liés à l'âge.
Conclusion
La reprogrammation cellulaire a démontré son potentiel non seulement en médecine régénérative, mais aussi dans le domaine du vieillissement grâce à l'amélioration des caractéristiques physiologiques et cellulaires du vieillissement. Cependant, la nature précise de la réjuvénation doit être pleinement comprise avant de pouvoir être mise en œuvre en toute sécurité en tant que traitement anti-âge. Par exemple, le suivi de toute trace de pluripotence dans des cellules partiellement reprogrammées (en particulier in vivo) est une précaution nécessaire pour minimiser le risque de cancer à long terme. De plus, ce phénotype reste-t-il stable ou finit-il par se détériorer à un rythme plus rapide que le vieillissement normal ?
D'autres préoccupations importantes en matière de sécurité réjuvénation incluent la façon dont les facteurs de reprogrammation sont introduits in vivo. Les rétrovirus sont couramment utilisés pour intégrer des facteurs de reprogrammation dans le génome. Cependant, cette méthode comporte des risques. Les méthodes de délivrance telles que la transfection d'ARN sont des alternatives plus sûres. Une autre alternative sûre est la reprogrammation chimique, qui implique la conversion directe d'une cellule somatique en un état pluripotent en utilisant de petites molécules et des facteurs de croissance. Il évite également l'utilisation de c-Myc, qui est un oncogène.
Une analyse plus approfondie est également nécessaire concernant les cellules pré-malignes, qui ont une propension plus élevée à se transformer en un état malin, après la réjuvénation.
Il reste également à explorer plus avant si et comment réjuvénation fonctionnerait sur les cellules différenciées en phase terminale post-mitotiques, telles que les neurones, les cardiomyocytes ou les adipocytes, mais également sur d'autres cellules ne se divisant pas telles que les cellules quiescentes ou sénescentes. Cette question est particulièrement importante dans la cadre de la SLA car les motoneurones sont des cellules quiescentes. Des travaux pilotes ont été réalisés dans ces deux derniers états, démontrant qu'un phénotype rajeuni est réalisable après restauration de la division cellulaire. Ces résultats pourraient indiquer un scénario où la prolifération est une exigence essentielle pour le rajeunissement. En effet, la pluripotence induite des neurones postnatals n'est possible qu'après une prolifération cellulaire forcée via l'expression de p53.
Cet article est adapté à partir de cette publication
doi: 10.1186/s13148-021-01158-7
Cellular reprogramming and epigenetic rejuvenation
Daniel J. Simpson, Nelly N. Olova, et Tamir Chandra


 Les chercheurs ont appliqué divers prédicteurs d'âge à une reprogrammation bien étudiée de 49 jours sur des fibroblastes dermiques humains (HDF) qui contenaient à la fois des données de méthylation (pour suivre l'âge comme indicateur de l'âge biologique) et des données d'expression génique (pour suivre les marqueurs cellulaires comme un proxy pour l'identité somatique).
Les chercheurs ont appliqué divers prédicteurs d'âge à une reprogrammation bien étudiée de 49 jours sur des fibroblastes dermiques humains (HDF) qui contenaient à la fois des données de méthylation (pour suivre l'âge comme indicateur de l'âge biologique) et des données d'expression génique (pour suivre les marqueurs cellulaires comme un proxy pour l'identité somatique). Moreover, they identified two genetic variants shared in the two studies conducted on FTD and ALS. These two variants are located in two genes that encode proteins with role in RNA metabolism which is a well-documented pathological mechanism operating in these disorders.
Moreover, they identified two genetic variants shared in the two studies conducted on FTD and ALS. These two variants are located in two genes that encode proteins with role in RNA metabolism which is a well-documented pathological mechanism operating in these disorders.
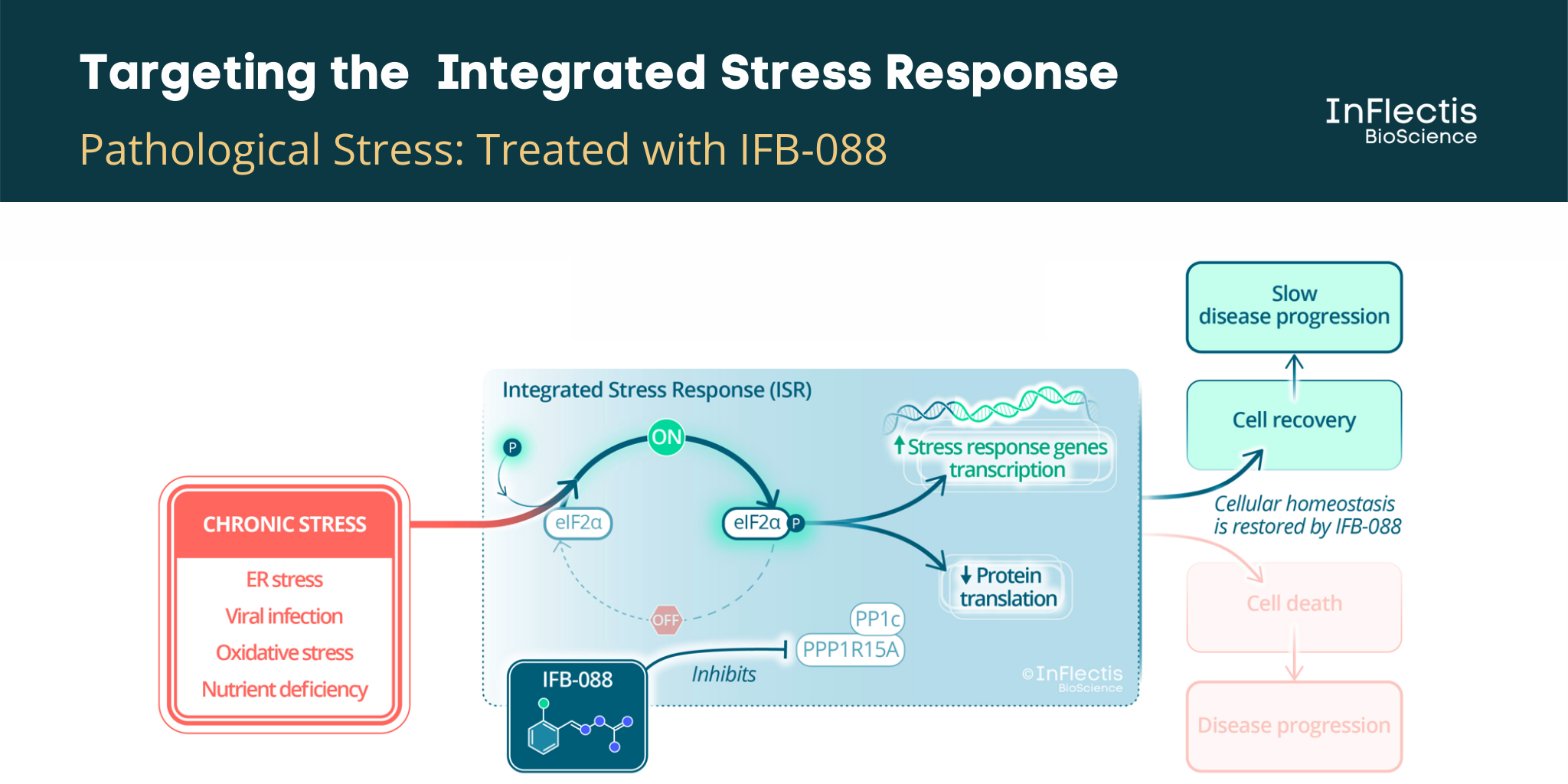 In a phase II clinical trial in Italy, Guanabenz offered a comparable level of protection to AMX0035 for people but specifically for patients with a bulbar onset.
In a phase II clinical trial in Italy, Guanabenz offered a comparable level of protection to AMX0035 for people but specifically for patients with a bulbar onset.