ALS and cancer
There is a persistent mystery about the causative mechanisms of ALS. The intense work over the last two decades on SOD1 has not helped to conclusively understand its link with the disease. Many SOD1 mutations produce very similar ALS phenotypes. But these mutations have not prevented neurons from functioning properly for several decades, so it is difficult to invoke them to explain the onset of the disease. Even though there is less scientific work on FUS or TDP-43, as their discovery is more recent, the mystery is also complete on how a non-mutated and mis-located TDP-43 protein in the cytoplasm could kill a neuron. The only obvious case is that of C9orf72, where the dipeptide repeats, clearly could not produce functional protein. However, even in this case, it is unclear why ALS only occurs at an advanced age.
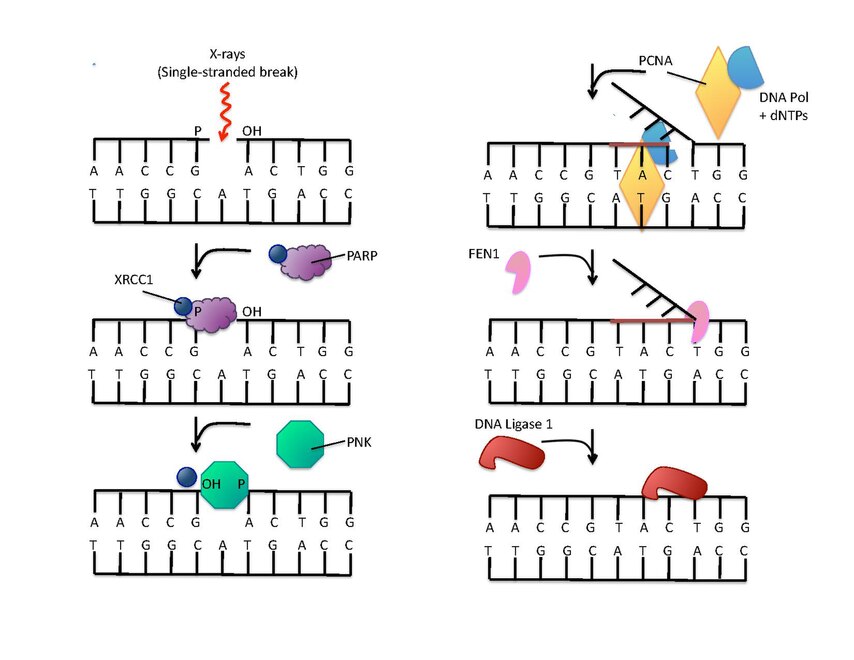
PARP is involved in DNA repair
There is a troubling link between cancer and ALS, for example, there is an inverse relationship between the onset of cancer and the onset of ALS. ALS medications also have anti-cancer properties. So, perhaps it's not surprising that they can share a fundamental cause: defects in DNA repair mechanisms. Poly-ADP-ribose polymerases (PARPs) are involved in DNA repair, as are FUS or TDP-43.
During DNA damage or cellular stress, ** PARP ** is activated, resulting in an increase in the amount of poly-ADP-ribose and a decrease in the amount of NAD +.
The poor localization of FUS and TDP-43 in the cytoplasm inhibits the mechanism of DNA repair
FUS and TDP-43 both play a role in the treatment of RNA, including splicing, transcription and transport. The involvement of FUS and TDP-43 in the response to cell genome damage has recently been discovered. In healthy neurons, FUS protects the genome by facilitating dependent recruitment of ** PARP-1 **. The authors report that TDP-43 is an essential component of the end-junction-mediated double-stranded DNA (DNA) repair pathway (NHEJ). TDP-43 is rapidly recruited to double-stranded DNA sites to stably interact with DDR and NHEJ factors, acting in particular as a scaffold for recruitment of the isolating XRCC4-DNA ligase 4 complex at DSB sites. Indeed, the presence of fragmentation of TDP-43 and its aggregation in ALS samples is strongly correlated with the presence of ** PARP-1 ** and cleaved caspase-3.
During apoptosis, PARP moves to the cytoplasm
Caspases are a family of cysteine proteases that play an essential role in programmed cell death. This protease cleaves ** PARP-1 ** into two fragments, leaving it completely inactive to limit the production of poly-ADP-ribose. One of its fragments migrates from the nucleus to the cytoplasm and is considered a target of autoimmunity. At the beginning of 2019, dysregulation of PARylation was found to contribute to the pathogenesis of ALS by promoting protein aggregation.
Although PARylation occurs primarily on PARP proteins, the association of PAR with ALS-related granules has been observed.
Causal chain of ALS
The results of the scientists thus link the pathology of TDP-43 to altered repair of DSB and persistent DDR signaling in motor neuron diseases, and suggest that targeted therapies on double-stranded DNA repair could improve genome instability induced by the toxicity of TDP-43 in motor neuron diseases.
In summary the mechanism causing TDP-43 ALS would be:
- Mutations of FUS or TDP-43 would render DNA repair ineffective.
- The intervention of PARP would repair this DNA and relocate TDP-43 in granules in the cytoplasm.
- This would further aggravate the problems of DNA repair.
A possible therapeutic mechanism
These new findings provide insight into how a DNA repair defect may be associated with FUS and / or TDP-43 neurodegeneration, and raises the question of whether the resolution of DNA ligation problems would be a pathway. promising for the development of neuroprotective treatments.
So mechanisms that would alleviate the burden of PARP (which is different from inhibiting it), would improve the pathology.