The body's pH level is often stated to become slightly more acidic (below pH 7) as we age, but studies are inconsistent. Ideally, blood pH remains tightly regulated within a narrow range (around 7.4). This is crucial for many bodily functions. It's less clear how the brain's PH is modified with aging and disease. A collaborative research group comprising 131 researchers from 105 laboratories mostly from Japan has published an impressive paper in eLife on the influence of brain pH and lactate levels in neurological disorders. The research group's previous findings in a 2018 small study, suggest that the brain's PH alteration is a consequence of diseases. This conclusion was drawn from five animal models of schizophrenia/developmental disorders, bipolar disorder, and autism.
The recent study, suggests that changes in brain pH and lactate levels are a common feature in a diverse range of animal models of diseases, including schizophrenia/developmental disorders, bipolar disorder, autism, as well as models of depression, epilepsy, and Alzheimer's disease.
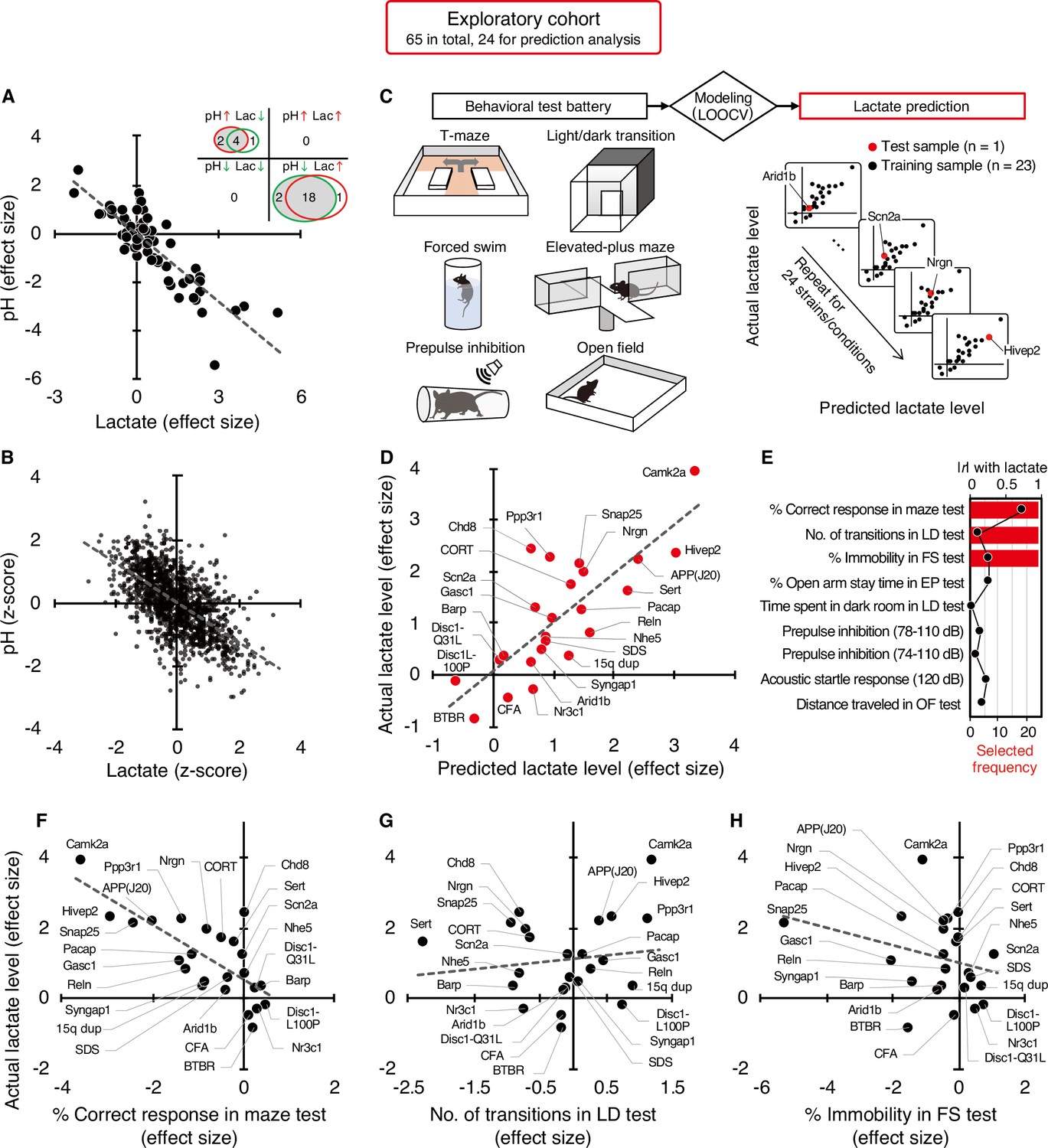 What could be the mechanism between increased lactate and decreased pH?
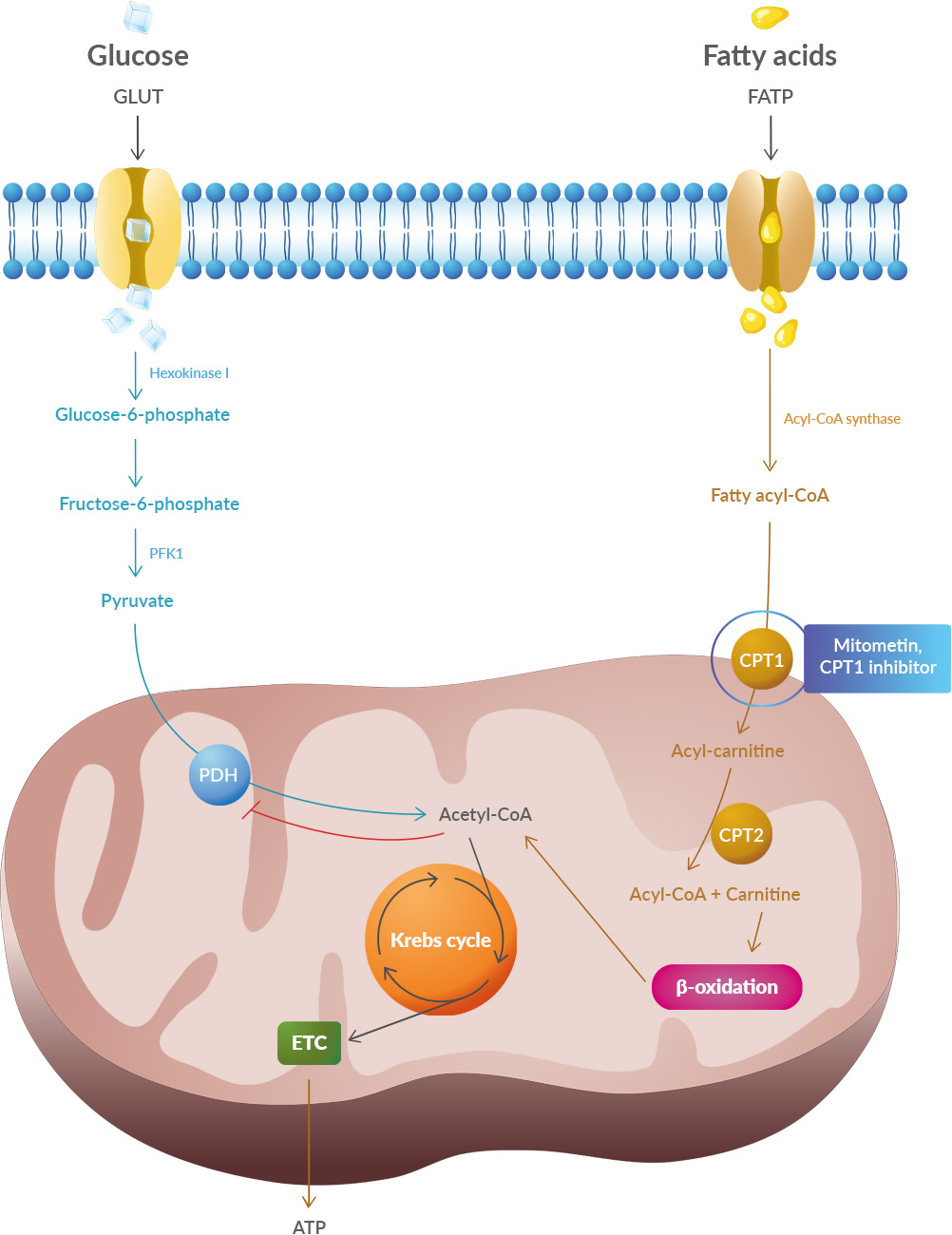
Lactate is a byproduct of metabolism and it is an acid, hence the acidification of pH. Neuronal activity relies heavily on glucose for energy. Under normal conditions, oxygen is readily available, and glucose is broken down through aerobic respiration, producing ATP (energy) with minimal lactate as a byproduct. However, during periods of high neuronal activity or limited oxygen supply, cells shift to anaerobic metabolism, relying more on glycolysis. This process produces more lactate as a byproduct.
What could be the mechanism between increased lactate and decreased pH?
Lactate is a byproduct of metabolism and it is an acid, hence the acidification of pH. Neuronal activity relies heavily on glucose for energy. Under normal conditions, oxygen is readily available, and glucose is broken down through aerobic respiration, producing ATP (energy) with minimal lactate as a byproduct. However, during periods of high neuronal activity or limited oxygen supply, cells shift to anaerobic metabolism, relying more on glycolysis. This process produces more lactate as a byproduct.
These changes were observed in the postmortem brains of patients deceased of several neurological diseases, including Alzheimer's disease. However, the observed phenomena are potentially confounded by secondary factors such as the administration of antipsychotic drugs. In addition, the brains of deceased patients have undergone multiple changes during the transition between life and death, and the conservation process, and these postmortem brains may not reflect the condition of living patients.
This time the authors included autism, epilepsy, bipolar disorder, autism, models of depression, epilepsy, and Alzheimer's disease, as well as peripheral diseases or conditions comorbid with psychiatric disorders (e.g. diabetes mellitus [DM], colitis, and peripheral nerve injury). These animal models included 109 mice, rats, and chick animal models with genetic modifications, drug treatments, and other experimental manipulations such as exposure to physical and psychological stressors. More than 2200 animals were used in a hundred laboratories.
First, this large-scale animal model study revealed that alterations in brain pH/lactate levels can be found in approximately 30% of the animal models examined. 30% is not 100% so more studies are needed to understand this result.
The authors observed no significant correlation between brain pH and age in the wild-type/control rodents. In human studies, inconsistent results have been obtained regarding the correlation between brain pH and age. There isn't necessarily a direct cause-and-effect relationship between aging and altered pH, but rather a decline in the body's efficiency to maintain homeostasis (stable internal environment).
- Reduced Kidney Function: Kidneys play a key role in balancing blood pH by filtering out acids. As kidney function declines with age, the body may struggle to eliminate excess acid: Drink more, and quality water with low minerals!
- Decreased Metabolic Activity: A lower metabolic rate can lead to the buildup of acidic byproducts in the body. Decreased Metabolic Activity manifests itself in slower digestion, heart rate, and breathing, lower body temperature, and reduced strength.
So the authors conclude that if this correlation between brain pH and age, is a feature of disease and not aging, then brain diseases might be instrumental in the appearance of these changes in pH in the brain, but the mechanism of action is far from clear.
Their analysis found that poorer working memory performance in animal models of neuropsychiatric disorders may be predominantly associated with higher lactate levels, which was confirmed in an independent cohort. They found the same result for anxiety, probably because it causes a large increase in brain activity.
In conclusion, this is an excellent study, there are too few studies of that caliber. In the future research will improve the brain's ability to remove lactate. This might involve stimulating transporters that clear lactate from the CNS or potentially using enzyme therapies to convert lactate into other metabolites. Another possibility is with therapies that encourage the brain to rely more on aerobic respiration (oxygen-dependent energy production) as they could minimize lactate production as a byproduct. This could involve optimizing blood flow to the brain or exploring potential metabolic drugs.

 Improving cognition using a simple probiotic would be an extraordinary result due to its simplicity of implementation.
Improving cognition using a simple probiotic would be an extraordinary result due to its simplicity of implementation.
 Studies have shown that oxidative stress and endoplasmic reticulum stress are correlated and can lead to protein misfolding (Abramov et al., 2020). Accumulation of misfolded proteins causes cellular damage and mitochondrial dysfunction and is associated with a range of neurodegenerative diseases, including ALS (misfolded SOD1, TDP-43, C9orf72) (McAlary et al., 2020), Parkinson's disease (misfolded α-synuclein) and Alzheimer disease (misfolded Aβ and Tau) (Abramov et al., 2020).
Studies have shown that oxidative stress and endoplasmic reticulum stress are correlated and can lead to protein misfolding (Abramov et al., 2020). Accumulation of misfolded proteins causes cellular damage and mitochondrial dysfunction and is associated with a range of neurodegenerative diseases, including ALS (misfolded SOD1, TDP-43, C9orf72) (McAlary et al., 2020), Parkinson's disease (misfolded α-synuclein) and Alzheimer disease (misfolded Aβ and Tau) (Abramov et al., 2020).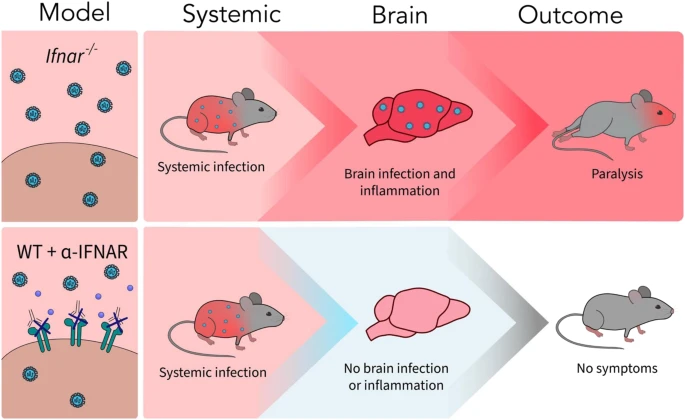 A new article aims to show that in the case of Zika viruses,
A new article aims to show that in the case of Zika viruses, 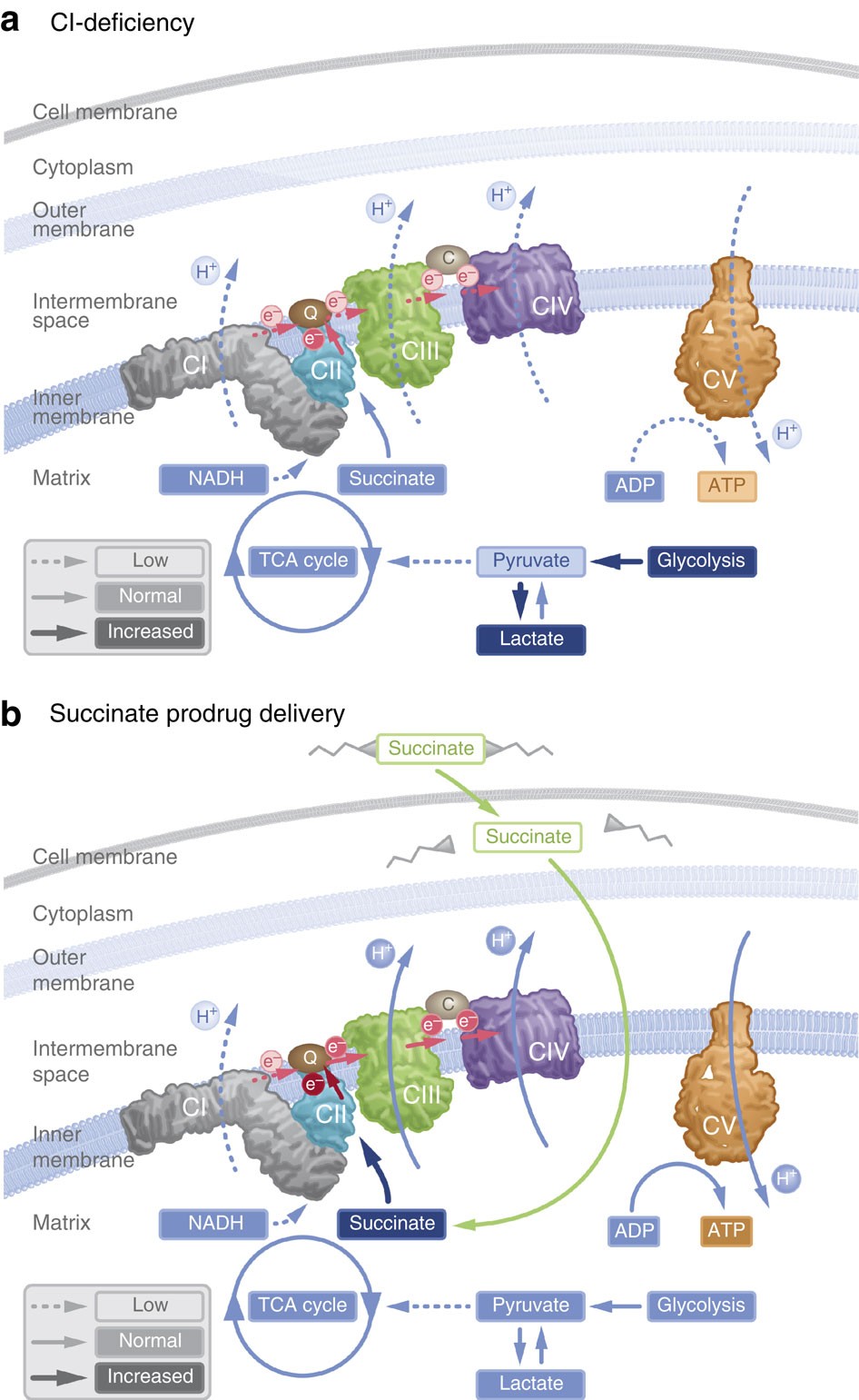 In particular, supplementation with dimethyl succinate, a substrate bypassing the inhibited step in the TCA cycle, suggests a potential therapeutic strategy to mitigate mitochondrial dysfunction in Alzheimer's disease. Dimethyl succinate (DMS), a membrane-permeant form of succinate, could serve as a pro-drug to provide substrate to the next enzymatic step in the TCA cycle, succinate dehydrogenase (SDH).
In particular, supplementation with dimethyl succinate, a substrate bypassing the inhibited step in the TCA cycle, suggests a potential therapeutic strategy to mitigate mitochondrial dysfunction in Alzheimer's disease. Dimethyl succinate (DMS), a membrane-permeant form of succinate, could serve as a pro-drug to provide substrate to the next enzymatic step in the TCA cycle, succinate dehydrogenase (SDH). The authors believe that an impaired blood-brain barrier allows immune cells from the body to pass through, which leads to the activation of microglia in the central nervous system. Scientists point out that immune processes intensively consume energy, therefore glucose, and therefore insulin resistance slows down immune processes.
The authors believe that an impaired blood-brain barrier allows immune cells from the body to pass through, which leads to the activation of microglia in the central nervous system. Scientists point out that immune processes intensively consume energy, therefore glucose, and therefore insulin resistance slows down immune processes. .
(source:
.
(source: