Un nouvel article dans la revue BioSocieties, publié par les Drs. Shlomo Guzmen-Carmeli et David A. Rier, du département de sociologie et d'anthropologie de l'Université Bar-Ilan, raconte l'histoire de CliniCrowd, une société israélienne créée pour tester l'efficacité de suppléments nutritionnels comme le mannitol, la cannelle ou les cerises dans les maladies de Parkinson ou d'Alzheimer.
Le modèle de CliniCrowd met l'accent sur la vitesse, l'efficacité et la créativité pour traiter un type particulier de science inachevée, impliquant des médicaments orphelins potentiels qui, d'origine naturelle, ne peuvent pas être brevetés.
En effet les questions scientifiques n'ont pas toutes les mêmes chances d'être explorées par les scientifiques officiellement accrédités.
Le terme de « science inachevée » fait référence en sociologie aux domaines de recherche identifiés par les mouvements sociétaux comme ayant des impacts sociaux potentiellement importants qui ne sont pourtant pas financés, ou incomplets ou encore complètement ignorés. Ces recherches, bien que souvent initiées ne sont finalement pas réalisées pour des raisons financières, théoriques, idéologiques, ou encore politiques.
Le modèle classique de Parsons (1951) du rôle de malade du patient suppose que toute l'action réside chez le médecin (l'expert), qui agit sur les patients passifs qui restent eux-même passifs, car à priori incompétents.
Cependant cela a évolué vers la fin du XX siècle, en particulier avec la lutte contre le SIDA. En 1987, l'Initiative de recherche communautaire, un partenariat de médecins et de patients communautaires, a commencé un essai clinique de base sur la pentamidine en aérosol comme traitement de la pneumonie à pneumocystis, alors la principale menace pour les patients atteints du SIDA.
L'essai a fourni des données cliniques importantes, a rapidement influencé la pratique clinique et a même été utilisé par la Food and Drug Administration (FDA) des États-Unis dans le processus d'approbation.
Les militants ont également formé des groupes pour identifier et obtenir (parfois, via la contrebande) des traitements potentiels non disponibles aux États-Unis. Ils ont critiqué les sociétés pharmaceutiques pour leurs prix élevés et leur incapacité à étudier une gamme plus large de composés. Ils ont particulièrement attaqué la dépendance de la FDA à des essais cliniques randomisés très lents et coûteux (le «gold standard» traditionnel).
En 2004, Le site communautaire PatientsLikeMe avait été lancé par deux frères et un ami d'un patient atteint de sclérose latérale amyotrophique (SLA). Il a ouvert ses portes en 2006 en tant que plate-forme en ligne, permettant aux patients atteints de SLA de mettre en commun leurs données cliniques téléchargées et anonymisées, d'évaluer leurs propres progrès, d'échanger des conseils et de l'assistance, et de contribuer plus généralement aux connaissances cliniques émergentes sur la maladie.
Finalement, PatientsLikeMe est actuellement une entreprise à but lucratif, car rachetée en 2019 par une grande société de gestion des soins. Ils vendent des données agrégées et anonymisées à des clients universitaires et professionnels tels que des sociétés pharmaceutiques et de dispositifs médicaux.
En Israël, les élites de la défense et des start-up high-tech sont souvent considérées parmi les plus brillantes et les plus innovantes de la société, car formées pour penser de manière créative, collaborer et prendre des risques.
Dan Vesely, est un général israélien à la retraite et un entrepreneur en haute technologie. Voici comment il décrit sa réponse à son terrifiant diagnostic de maladie de Parkinson en 2013 :
"If there’s a problem, deal with it. No crying over spilled milk or grieving about my misfortune, about what I ‘won’ [said cynically]. Come on, what do we do next? We think of solutions. [interview, January 24, 2018]"
Vesely, évidemment insatisfait des options de traitement qui lui était proposées, a alors demandé de l'aide à des connaissances. Un petit groupe d'entrepreneurs s'est réuni autour de lui pour rechercher les recherches publiées sur la maladie de Parkinson.
Ils ont rapidement remarqué l'étude publiée - et oubliée - sur l'effet possible du mannitol sur les patients atteints de la maladie de Parkinson. Vesely et certains partenaires ont contacté le professeur Dan Segal de l'Université de Tel-Aviv, qui avait co-dirigé l'équipe de recherche, et ont demandé à le rencontrer :
"It had not yet been tested on humans. So I made an appointment....Prof. Segal told us his story, described the experiment, and said it's all simply been shelved, there’s no incentive for the pharmaceutical companies. We looked at each other and said, ’So we’ll take it!’ The professor said, ’Who exactly are you? You brash Israelis, who are you?’ But it was clear to us that if you can’t go through the door, you go through the window. [Vesely interview, Jan. 24, 2018]"
L'histoire navrante de l'étude abandonnée a affecté le groupe d'amis. Vesely a résolu alors de tester le mannitol sur lui-même. Cependant, ses partenaires l'en ont dissuadé comme étant inefficace pour la communauté car totalement inconcluant. Au lieu de cela, ensemble ils ont décidé de tester le mannitol sur un certain nombre de patients atteints de la maladie de Parkinson.
Faute de l'appui d'une entreprise pharmaceutique prête à investir dans la recherche clinique, ils ont alors cherché à tester le mannitol comme s'il s'agissait d'une opération militaire.
Ils ont adopté un modèle, mariant l'auto-expérimentation du patient avec des techniques de crowdsourcing. Inspiré par des projets de crowdsourcing similaires comme PatientsLikeMe, le groupe a alors projeté de créer un site Web pour les patients atteints de la maladie de Parkinson qui accepteraient de prendre régulièrement du mannitol pendant une période prolongée.
Cette alternative n'est cependant pas un véritable substitut aux essais cliniques « classiques ». La plate-forme d'enquête manquerait en effet d'un groupe de contrôle et la surveillance des patients serait effectuée sur le site de manière volontaire et indépendante, et non par un médecin.
Néanmoins, cette plate-forme d'enquête générerait des données préliminaires permettant de justifier la nécessité d'une recherche clinique plus formelle ce qui serait un résultat d'une grande valeur en soi.
Les fondateurs de CliniCrowd ont initialement envisagé de commercialiser directement le mannitol, mais ont décidé de ne pas le faire, pour éviter les conflits avec leurs recherches. Mais les fondateurs de CliniCrowd ont néanmoins choisi de l'enregistrer en tant que société plutôt qu'en tant qu'organisation à but non lucratif. Cela reflétait leur motivation principale de « faire le travail » aussi rapidement et efficacement que possible, via des tactiques entrepreneuriales, plutôt que d'adopter l'identité et les tactiques de l'activisme social. Par ailleurs, les organisations à but non lucratif israéliennes sont davantage réglementées que les sociétés commerciales.
Ils ont donc créé la société en août 2016. Ils ont recruté du personnel qualifié expérimenté dans la planification et la conduite d'essais cliniques pour créer la plate-forme de l'entreprise, puis ont commencé à recruter des patients à l'aide de forums de patients et d'une exposition médiatique.
Début 2021, 2 480 patients s'étaient inscrits sur la plateforme dédiée à la recherche de mannitol pour la maladie de Parkinson. Parmi ceux-ci, 1 364 (55 %) avaient rempli des questionnaires à plusieurs reprises. La plateforme permet aux patients d'enregistrer et de suivre les données liées à leur maladie et (tout en préservant l'anonymat) de comparer ces données avec celles d'autres membres de la communauté. Il est également possible de partager les données stockées avec le médecin traitant.
Les efforts de CliniCrowd se sont déployés en plusieurs étapes. Alors que les patients atteints de la maladie de Parkinson sur la plate-forme commençaient à prendre du mannitol et à remplir régulièrement des questionnaires sur leurs symptômes, l'étape suivante était d'attirer des scientifiques accrédités pour mener des essais plus importants.
Les données initiales de CliniCrowd ont permis de susciter une pression publique, menant à son tour à une étude clinique formelle, lancée en 2018 au centre médical Hadassah à Jérusalem. Cette étude (https://clinicaltrials.gov/ct2/show/NCT03823638), menée avec un financement public, examine les effets du mannitol sur la maladie de Parkinson. En juin 2021, l'étude se poursuivait, mais avait quelque peu ralenti en raison du coronavirus et de son grave impact sur le système médical. Des études supplémentaires, dans des universités et des centres médicaux au Royaume-Uni et aux États-Unis, devraient commencer sous peu. Pour autant que les auteurs de cet article le sachent, au moment de la rédaction, il s'agit cependant d'études limitées.
Néanmoins, il y a déjà eu un revirement important concernant la façon dont les scientifiques considèrent la recherche sur le mannitol. Comme l'a fait remarquer Vesely, le patient-fondateur de CliniCrowd :
"It gives me great satisfaction that the studies we are currently talking about [the clinical research underway in Jerusalem and expected further studies] would not have taken place, nor would they have received funding or the attention of the medical establishment and the public, without the buzz and especially the clinical indications that CliniCrowd achieved in the wake of the surveys. [interview, July 7, 2019"
Les chercheurs impliqués dans la planification de l'essai clinique ont confirmé lors d'entretiens avec les auteurs que, sans la pression exercée par le public, il est peu probable qu'un essai ait été initié.
En fait, la position de CliniCrowd vis-à-vis de l'establishment biomédical a évolué au cours de sa courte histoire. Dans les premiers entretiens, les fondateurs ont vivement critiqué l'industrie pharmaceutique. Par exemple, dans le premier entretien avec le PDG Amir Sadeh, il décrit ainsi la décision de créer l'entreprise :
"The goal is to create something that cannot be ignored and make available to the public what the pharmaceutical companies are trying to hide from us. Because they [such ‘ignored’ compounds] do not generate income, they do not make a profit, so it’s better not to know about them at all. But now we’re exposing them, showing their nakedness in public, telling them it's inexpensive and accessible. It treats the cause rather than the symptoms, and that’s why it’s the worst thing for the pharmaceutical companies to find a solution to Parkinson's disease. Ten million people, five billion dollars a year—as far as they’re concerned, let's just treat the symptoms. It's cynical but that's the way it is…. [T]he benefit of the patients is not the paramount interest of the companies or the doctors, because they are waiting for the next seminar in the Seychelles, courtesy of one company or another. [interview December 3, 2017]"
Pourtant, cette position initiale de « rebelles contre l'industrie pharmaceutique" a été créée par des membres d'élite de l'establishment israélien,
Avec cette approche, CliniCrowd a évidemment éprouvé des difficultés à obtenir la confiance et le soutien de l'establishment médical.
D'après les entretiens que les auteurs ont menés avec des patients qui ont commencé à prendre du mannitol entre 2016 et 2018, il apparaît que ceux qui ont consulté leur médecin ont rencontré une résistance substantielle à l'adoption du mannitol comme remède. Les objections des médecins comprenaient des commentaires tels que : « c'est un remède de bonne femme » et « vous feriez mieux d'obtenir la bénédiction d'un rabbin ».
Lors d'une conférence de neurologues au début de 2017, les délégués de CliniCrowd n'ont eu que quelques minutes pour présenter leur action, et la plupart des participants à la conférence ont ignorés leur discours. Un tel mépris rappelle l'opposition contre la production communautaire de connaissances sur le SIDA il y a plus d'une génération.
Les interviews ont clairement montrés que le choix d'adopter des termes tels que « compléments alimentaires » et « aliments fonctionnels » reflète la décision tactique de CliniCrowd de redéfinir le mannitol comme une nouvelle substance dans l'alimentation marché des suppléments.
Voici comment le PDG Sadeh a décrit le changement, dans une interview de suivi :
"We started out thinking we would call the venture Ampha, as opposed to Pharma. But the more we got into it, the more we realized that was not the point. Like Netflix doesn’t mean all movie theatres are closed, and Airbnb hasn’t replaced hotels, and Uber hasn’t replaced taxis, so CliniCrowd won’t replace the pharmaceutical companies. We fill a void and add something extra. If we started out by setting ourselves against the pharmaceutical companies, now we’re not against them, we’ll be in favour. We’ll complement them. Let’s shift the playing field. Instead of acting on the fiery and aggressive pharmaceutical playing field, let’s move the field elsewhere....And as long as the whole world of medicine doesn’t dance according to the interests of the pharmaceutical companies, we’ve done something great. [interview July 7, 2019]"
Le changement d’appellation du mannitol en tant qu'aliment fonctionnel s'est avéré une manœuvre précieuse, permettant à CliniCrowd. Cela a contribué à promouvoir l'acceptation du mannitol parmi les médecins et les patients.
En effet, au second semestre 2018, les auteurs ont constaté un changement d'attitude chez les médecins. Trois médecins interrogés pour l'étude nous ont dit qu'une fois qu'ils ont compris qu'il s'agissait d'un complément alimentaire, ils ont cessé de protester : « *C'est un complément alimentaire. Cela n'aide peut-être pas, mais ce n'est pas nocif » *.
Comme l'explique un neurologue :
"I think no doctor likes it when the patient comes and says, ‘Listen, I’ve found a treatment.’ Most of the time I have to make sure his feet are on the ground, and I must explain why, most probably, in his case it won’t work. This was also my initial response to mannitol, complete resistance, not wanting them to take it....The attitude changes when there is already information and a mass of patients who have collated and documented its use in an orderly manner. Moreover, they didn’t come and say this is a magic drug, but rather that it may help with some of the symptoms....I suggest to patients, especially at the beginning, that they should read about mannitol. I definitely don’t exclude it, in fact quite the opposite."
Pour comprendre comment les patients eux-mêmes ont vécu cela, considérons Menachem [pseudonyme], 68 ans, diagnostiqué quatre ans plus tôt. Interrogé sur l'expérience de la prise de mannitol et de sa participation au questionnaire en ligne, il a répondu :
""My participation in the experiment has turned my world around. I come to the doctor and update him, see? I, Menachem, taught the neurologist that there is such a thing as mannitol, and that I am taking part in an experiment with other patients. When I go to see him, he immediately stands up! ‘Welcome’, he says, ‘tell me how you are getting on’. There is a sense that we are colleagues, and that I am doing something incredibly important. There is something in [mannitol] that helps, it’s not a magical cure, or maybe I no longer suffer. But there is an improvement in my sleep, my sense of smell, and also my difficulty in movement. [interview Oct. 30, 2019]"
Notez la facilité que Menachem décrit dans sa relation avec le médecin, son sentiment d'être un expert, son ravissement et l'agence qu'il ressent du fait de sa participation. Ceux-ci sont tous si importants pour lui qu'il les mentionne avant même son amélioration de la santé, qu'il attribue à la prise régulière de mannitol.
En conclusion, CliniCrowd a démontré une nouvelle façon d'aborder de la "science inachevée", en utilisant la recherche participative pour générer la pression et l'influence du public avec lesquelles attirer formellement les scientifiques pour tester des composés à faible potentiel de profit. CliniCrowd représente une intersection de connaissances scientifiques, de technologies, de pratiques,elle est aussi le produit d'un processus soutenu de diffusion et de décentralisation de l'expertise.
 The imaging analyzes that this study will produce, will make it possible to define a subgroup of patients with Parkinson's disease who will have benefited from the treatment and will help to define rules about when using this therapy in order to avoid unnecessary interventions.
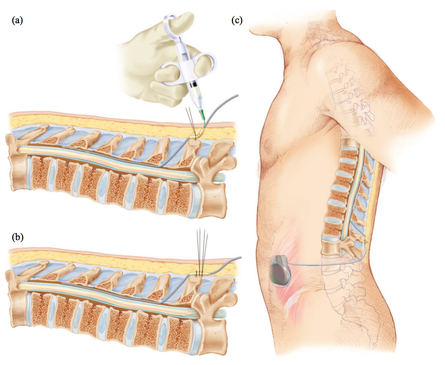
The imaging analyzes that this study will produce, will make it possible to define a subgroup of patients with Parkinson's disease who will have benefited from the treatment and will help to define rules about when using this therapy in order to avoid unnecessary interventions. Deep brain stimulation (DBS) is a neurosurgical procedure involving the placement of a medical device called a neurostimulator, which sends electrical impulses, via implanted electrodes, to specific targets in the brain (the cerebral nucleus) for treatment movement disorders, including Parkinson's disease. illness, essential tremor, dystonia, and other conditions such as obsessive-compulsive disorder (OCD) and epilepsy. Its underlying principles and mechanisms are not fully understood.
Deep brain stimulation (DBS) is a neurosurgical procedure involving the placement of a medical device called a neurostimulator, which sends electrical impulses, via implanted electrodes, to specific targets in the brain (the cerebral nucleus) for treatment movement disorders, including Parkinson's disease. illness, essential tremor, dystonia, and other conditions such as obsessive-compulsive disorder (OCD) and epilepsy. Its underlying principles and mechanisms are not fully understood.
 In this article, the authors outline the principles of drug selection for Parkinson disease prevention trials, focused on proof-of-concept opportunities that will help establish a methodological foundation for this fledgling field.
In this article, the authors outline the principles of drug selection for Parkinson disease prevention trials, focused on proof-of-concept opportunities that will help establish a methodological foundation for this fledgling field.