This study addresses a major debate regarding the causality of the C9ORF72 gene mutation in neurodegenerative diseases: does this mutation cause ALS and FTD via toxic RNA aggregates or toxic DPR proteins?
Traditionally considered distinct diseases, ALS and FTD share certain characteristics. In 2011, two research teams independently discovered that an abnormal repeat of the GGGGCC sequence in the C9orf72 gene is the most common genetic cause of ALS/FTD. In most people, this sequence is repeated between two and 20 times, but in some individuals, it can be repeated thousands of times. It is currently the most frequently observed mutation associated with ALS, far more common than SOD1, FUS, or TDP-43.
Ribonucleic acid (RNA) consists of a transient copy of a portion of DNA corresponding to one or more genes of a biological organism. mRNA is used by cells as an intermediary for protein synthesis. mRNA is a copy of DNA, comprising the coding region flanked by non-coding regions. It is synthesized as a precursor in the cell nucleus during a process called transcription. It then undergoes several maturation steps; some non-coding regions called introns may be excised during a process called splicing. The matured mRNA is exported to the cytoplasm where it is translated into protein by a ribosome. The information carried by mRNA consists of a series of codons, consecutive triplets of nucleotides, each of which codes for one amino acid of the corresponding protein. The sequence of these codons constitutes the gene itself, or cistron.
Normally, when a section of messenger RNA is converted into a protein, this section is delimited by a start codon and a stop codon. However, there is sometimes an abnormal conversion from an unconventional starting point, by translation of extended hexanucleotide repeats present in an intron of the C9orf72 gene, which produces short proteins called dipeptide repeat proteins (DPRs) that could be toxic.
However, the mechanism by which the expansion of the hexanucleotide repeat of the C9orf72 gene induces neurodegeneration remains poorly understood. An important question, therefore, is to determine whether it is the abnormal repeat of the GGGGCC sequence in the C9orf72 gene or the abnormal translation of the RNA of this gene that is toxic to neurons.
This study concludes that dipeptide repeat proteins (DPRs) are the main drivers of the disease, and not the RNA aggregates (foci).
Scientists have long struggled to separate these two factors, because DPRs are translated directly from the mutated RNA. To solve this problem, researchers used an ingenious gene-editing technique:
Target: They identified a specific start codon (CUG) that triggers the translation of the toxic proteins.
Modification: They replaced this CUG codon with CCG.
Result: The cell still produced the mutated RNA (and the resulting RNA foci), but it could no longer "read" the instructions necessary for the synthesis of the toxic DPR proteins.
 By testing this approach on mouse models of both diseases and on human patient stem cells (iPSCs), the team observed several crucial improvements:
By testing this approach on mouse models of both diseases and on human patient stem cells (iPSCs), the team observed several crucial improvements:
Behavior: Complete recovery of motor and cognitive deficits in mice.
Brain health: Reduction of neuroinflammation and significant increase in neuronal survival.
Biomarkers: Decreased levels of NfL (a protein released into the bloodstream upon neuronal death).
Cellular pathology: Elimination of TDP-43 aggregates, a "waste" protein characteristic of ALS/FTD.
This discovery opens a new chapter for potential therapies. Instead of tackling the complex challenge of eliminating all the mutated C9ORF72 RNA (which may have other vital functions), we can now focus on strategies to specifically target and block the production of these toxic DPR proteins.
Here’s how this could lead to future treatments:
CRISPR gene editing: The very technique used in this study—CRISPR base editing—could be harnessed for therapeutic purposes. Delivering a “molecular editor” to brain cells to change the critical CUG codon to CCG could be a one-time treatment that permanently prevents DPR synthesis. This would involve significant challenges in terms of delivery to the brain and ensuring specificity, but the potential is immense.
Antisense oligonucleotides (ASOs): These custom-designed molecules are already used in other neurological disorders. ASOs could be developed to bind specifically to RNA at or near the CUG start codon, physically blocking the cellular machinery of its translation into DPR.
Small molecule drugs: The pharmaceutical industry could search for small molecules capable of interfering with the RAN translation process itself, or of specifically targeting proteins involved in the initiation of DPR synthesis. This approach could be a more traditional, drug-analytical alternative.


 The researchers specifically focused on molecules that could reduce or reverse stress granule formation, particularly those that act directly on stress granule proteins and may be useful as therapeutic agents. From the initial screening, lipoamide emerged as a novel, potent modulator of stress granules.
Once lipoamide was identified as a hit, the researchers sought to determine its effects in cells regarding specificity, potency, intracellular localization, and its effects on other cellular condensates.
The researchers specifically focused on molecules that could reduce or reverse stress granule formation, particularly those that act directly on stress granule proteins and may be useful as therapeutic agents. From the initial screening, lipoamide emerged as a novel, potent modulator of stress granules.
Once lipoamide was identified as a hit, the researchers sought to determine its effects in cells regarding specificity, potency, intracellular localization, and its effects on other cellular condensates.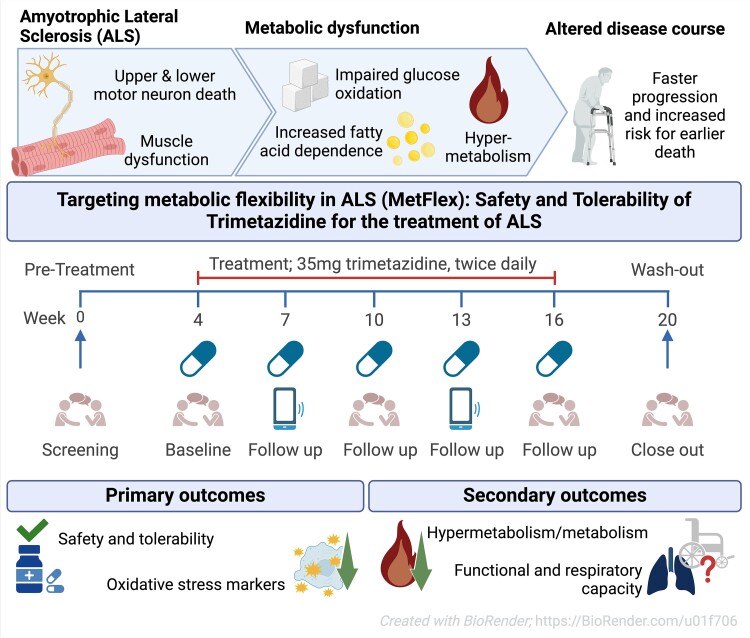 While the publication recounts that trimetazidine was beneficial for patients (this is not a phase III trial), for me the results section does not show conclusive results. For example, the results improved only during the wash-out period.
While the publication recounts that trimetazidine was beneficial for patients (this is not a phase III trial), for me the results section does not show conclusive results. For example, the results improved only during the wash-out period.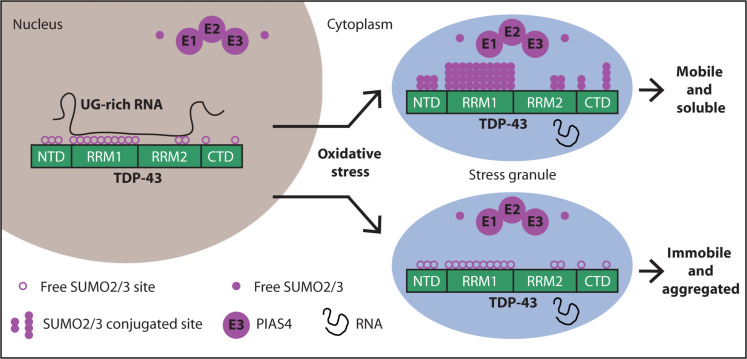 Transactive response DNA-binding protein 43 (TDP-43) is a nuclear RNA binding protein (RBP) involved in RNA metabolism.
TDP-43 has a high propensity to aggregate because of its low solubility in cells and in vitro.
The aggregation propensity of TDP-43 is increased by ALS/FTD-linked mutations and upon exposure to stress and has been observed in patients with C9orf72 hexanucleotide repeat expansion, the most common genetic cause of sporadic and familial.
Transactive response DNA-binding protein 43 (TDP-43) is a nuclear RNA binding protein (RBP) involved in RNA metabolism.
TDP-43 has a high propensity to aggregate because of its low solubility in cells and in vitro.
The aggregation propensity of TDP-43 is increased by ALS/FTD-linked mutations and upon exposure to stress and has been observed in patients with C9orf72 hexanucleotide repeat expansion, the most common genetic cause of sporadic and familial.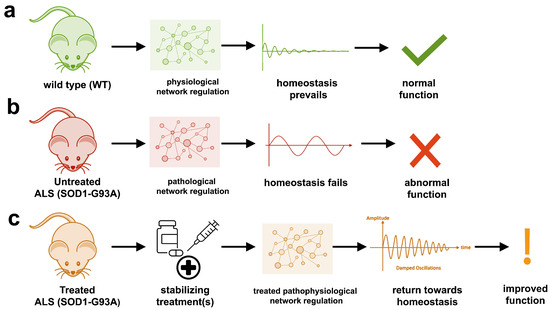 The study uses an innovative and integrative framework to model the regulatory dynamics of wild-type (WT) and SOD1-G93A ALS mice. The models are based on first-order ordinary differential equations (ODEs) that describe how the system output evolves over time. The research uses dynamic meta-analysis to synthesize experimental data from the literature and parameter optimization based on genetic algorithms to infer missing data. Indeed, to build a model, data are needed and here these are obtained from results reported in the literature on SOD1-G93A ALS mouse models.
The study uses an innovative and integrative framework to model the regulatory dynamics of wild-type (WT) and SOD1-G93A ALS mice. The models are based on first-order ordinary differential equations (ODEs) that describe how the system output evolves over time. The research uses dynamic meta-analysis to synthesize experimental data from the literature and parameter optimization based on genetic algorithms to infer missing data. Indeed, to build a model, data are needed and here these are obtained from results reported in the literature on SOD1-G93A ALS mouse models.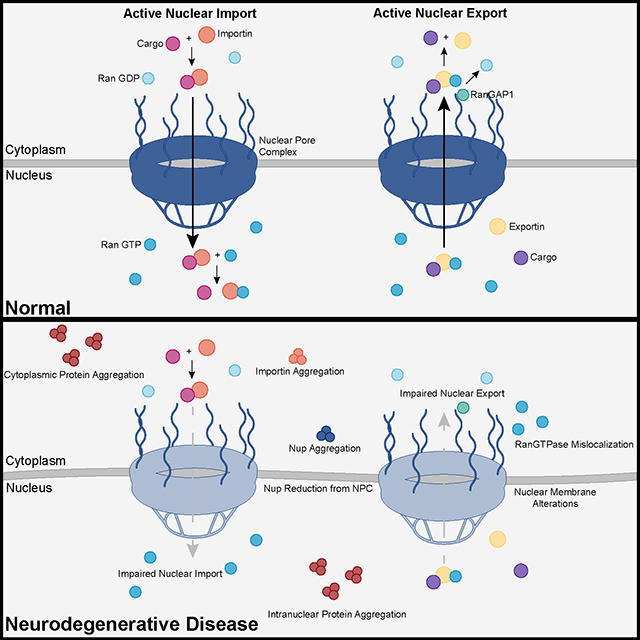 Recent advances into the underlying pathogenic mechanisms have associated mislocalization and aberrant accumulation of disease-related proteins with defective nucleocytoplasmic transport and its mediators called karyopherins.
Recent advances into the underlying pathogenic mechanisms have associated mislocalization and aberrant accumulation of disease-related proteins with defective nucleocytoplasmic transport and its mediators called karyopherins.